Fabriquer artificiellement, en éprouvette, ce qui ressemble à des embryons sans passer par la fécondation, sans ovule ou spermatozoïdes, est-ce possible ? Quelques laboratoires y travaillent, depuis quelques années déjà, sur des modèles animaux.
Des expériences sont aussi déjà menées avec des cellules humaines. Le projet de loi bioéthique, toujours en cours de révision, envisage d’autoriser ces recherches. (article 14 et 15), avec des modèles utilisant des cellules humaines adultes reprogrammées (IPS) et des cellules embryonnaires humaines. Ces protocoles de recherche seraient soumis à déclaration, et non à autorisation, à l’Agence de la biomédecine, préalablement à leur mise en œuvre.
En 2018, une équipe de Cambridge publiait déjà ses travaux. Cette semaine, ce sont deux autres laboratoires qui expliquent leurs recherches dans la revue Nature.
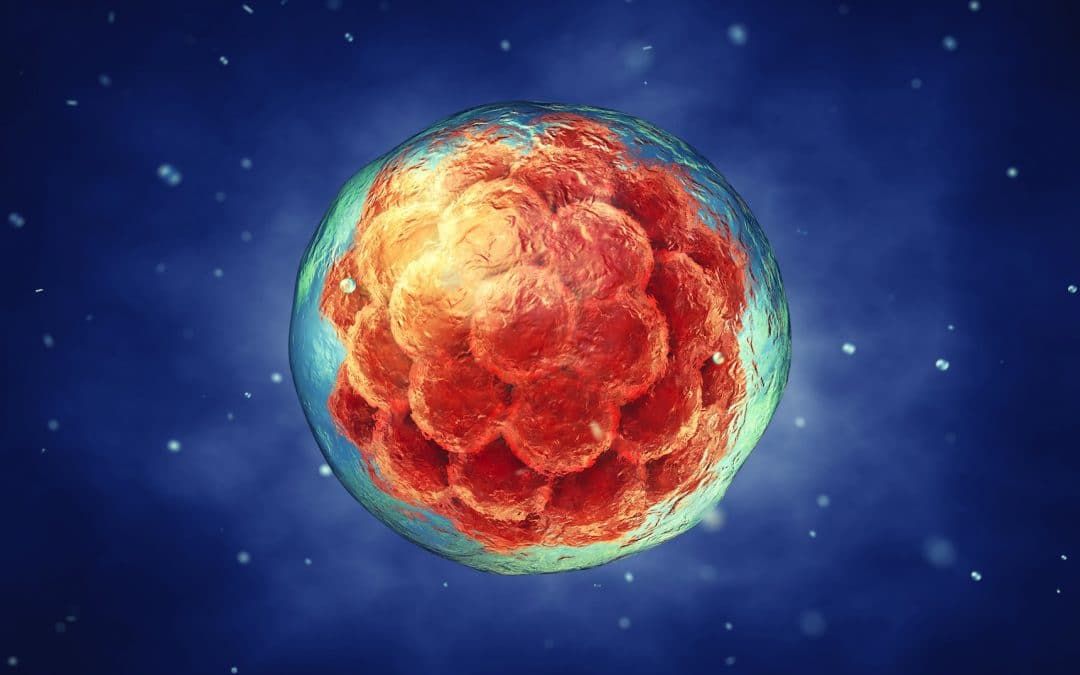
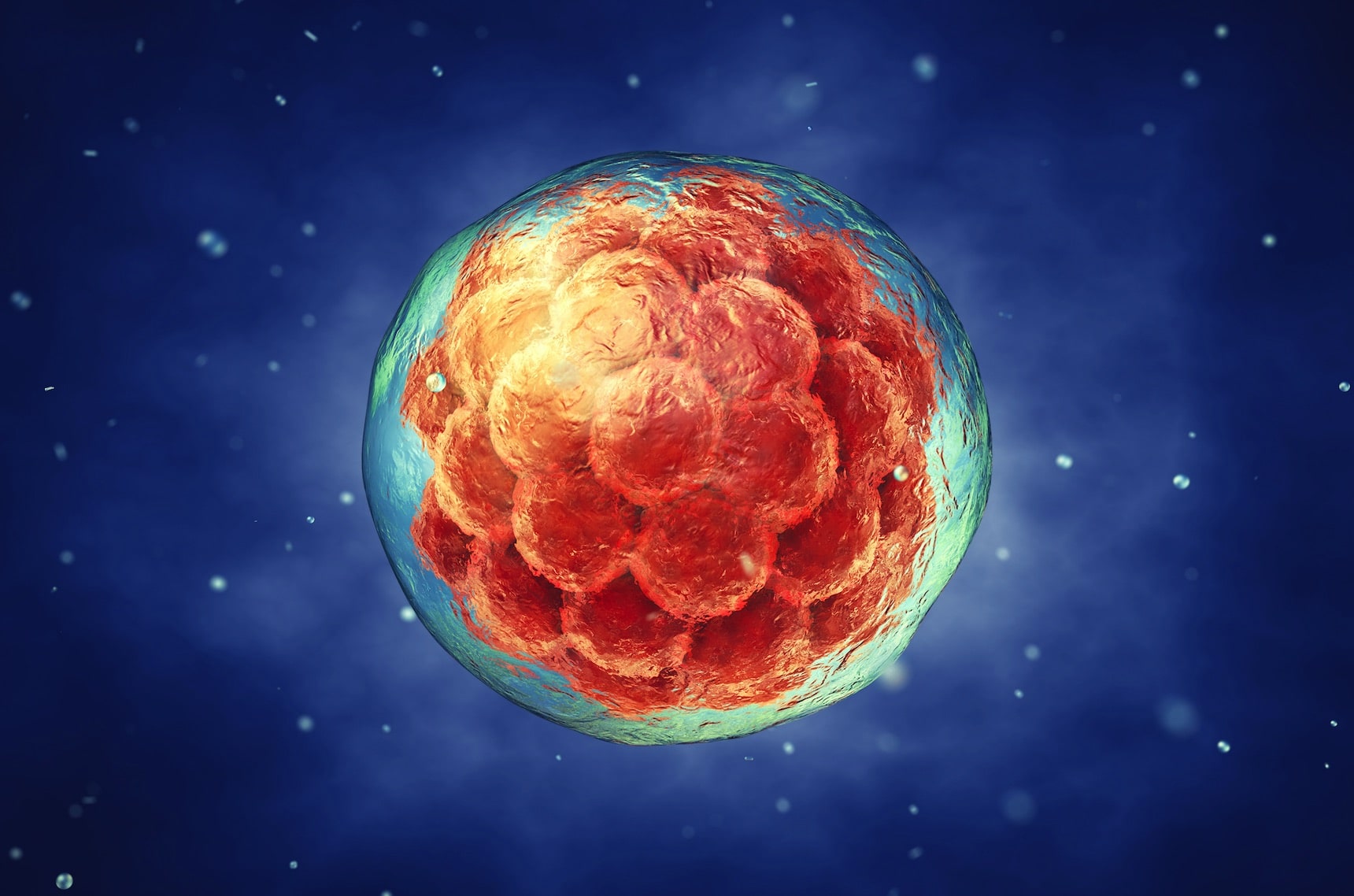
Ils travaillent à créer, in vitro, des structures organisées appelées « blastoïdes », pour rappeler le mot « blastocystes », nom scientifique donné à l’embryon humain âgé de cinq jours environ. Car ces structures fabriquées artificiellement entendent « imiter » les embryons humains.
Deux voies différentes ont été empruntées par deux équipes, une américaine et une australienne. L’équipe pilotée par José Polo, professeur à l’université Monash en Australie, a travaillé avec des fibroblastes, cellules de peau adultes. Ces cellules ont été « reprogrammées », par la technique dite « IPS » pour ré-acquérir leur capacité originelle de « pluripotence » (propriété de se différencier indéfiniment pour former la plupart des tissus de l’organisme).
L’autre équipe, dirigée par Jun Wu de l’université du Texas, a également utilisé ce type de cellules pluripotentes induites mais aussi des cellules souches embryonnaires humaines. Ces cellules sont des lignées établies à partir d’embryons humains, issus de Fécondation In Vitro (FIV) et ayant été (aban)donnés à la recherche.
Mises en culture dans un milieu favorable, ces cellules se sont multipliées et auto-organisées pour construire des structures cellulaires complexes. Pour l’organisation cellulaire en 3-dimensions, des supports ont été utilisés : ce sont des plaques en plastique creusées de « micropuits » qui servent à agréger les cellules par sédimentation, tout en contrôlant leur nombre.
Ces études confirment que les cellules « communiquent » entre elles puisqu’elles se sont auto-organisées en structures cellulaires composées de cellules différentes : une couche de cellules externes (figurant le futur placenta, s’il y avait fécondation et développement « normal ») entourant une cavité remplie de liquide qui contient une masse de cellules « embryonnaires ».
Mais ces structures artificielles présentent de notables différences avec leurs modèles naturels. Par exemple, elles contiennent des cellules absentes des véritables blastocystes. En 2018, le chercheur français Nicolas Rivron, responsable d’un laboratoire à l’Académie autrichienne des sciences, était parvenu à créer les premiers modèles de blastocystes de mammifère (souris). Pourtant, ce spécialiste estime qu’il faudra encore « dix ans pour créer des blastoïdes qui ressemblent fortement aux blastocystes humains ».
Ces structures ne peuvent se développer longtemps et il semble peu plausible qu’au stade actuel des recherches, elles aient la capacité de s’implanter dans l’utérus d’une femme, si l’expérience en venait à cette étape-là (procédure actuellement strictement interdite en France). Sur le modèle animal, l’expérience a déjà été menée. Les blastoïdes se sont implantés dans l’utérus de souris, des vaisseaux se sont connectés à ces structures pseudo-embryonnaires. Et le système immunitaire de la souris interagit avec eux. Mais, dès quatre jours après l’implantation, des anomalies dans ces structures ont été observées.
Les promoteurs de ces expériences voient plusieurs intérêts à ces recherches. Ces structures permettraient d’acquérir de nouvelles connaissances sur le développement précoce de l’embryon humain. Ces structures pourraient être des modèles pour tester la toxicité de molécules, comprendre des événements qui surviennent au début du développement embryonnaire comme les interruptions spontanées de grossesse ou les malformations favorisées par certains médicaments ou polluants. Avec une limite évidente : ce ne sont pas des embryons « normaux » et ils sont cultivés dans des milieux qui restent artificiels.
Ces modèles contournent l’interdiction de créer des embryons pour la recherche et sont présentés comme une alternative au recours à la recherche sur les embryons dits surnuméraires, particulièrement pour les modèles n’utilisant que des cellules adultes reprogrammées. Cependant, les hypothèses qui seront formulées grâce à ces modèles « devront être validées sur des embryons humains, et ne remplaceront donc pas la recherche sur les embryons issus de dons », estime Teresa Rayon, biologiste au Francis Crick Institute (Londres).
Concernant le statut juridique de « cette nouvelle catégorie d’objets vivants créés par l’être humain, nous sommes dans une zone grise », d’après Hervé Chneiweiss, président du comité d’éthique de l’Inserm.
L’article 17 de l’actuel projet de loi bioéthique, toujours en cours d’examen, a prévu une évolution sémantique notable d’un article du code de la santé publique (article L. 2151-2). Actuellement, cet article stipule que « La conception in vitro d’embryon ou la constitution par clonage d’embryon humain à des fins de recherche est interdite. ». Il est envisagé de compléter le mot « embryon », avec ces 5 mots : « humain par fusion de gamètes ». Ainsi, il est bien prévu que la porte législative s’ouvre à ce type d’ « embryons » obtenus sans fusion de gamètes.



![[CP] Alliance VITA lance une campagne d’affichage pour encourager les Français à rester reliés à leurs proches âgés ou isolés](https://www.alliancevita.org/wp-content/uploads/2021/03/Affiche-Visuel-Campagne-1080x675.jpg)